Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunologíaMicrobiología
TecnologíaIndustria
Eventos

- Herramienta de diagnóstico identifica múltiples condiciones de salud a partir de una sola gota de sangre
- Un analizador integrado de química e inmunoensayo con extenso menú de ensayos ofrece flexibilidad, escalabilidad y conmutabilidad de datos
- Prueba rápida de fármacos podría mejorar el tratamiento de pacientes que se presentan en el hospital
- Modelo de IA detecta el cáncer a una velocidad relámpago mediante análisis de azúcar
- El primer chip alimentado por sangre ofrece monitoreo de salud en tiempo real
- Panel de biopsia líquida para tratamiento de cánceres pediátricos
- Prueba por punción digital detecta Alzheimer de forma temprana
- Análisis de sangre más inteligentes permiten diagnósticos más rápidos y mejores resultados
- Una única prueba de secuenciación metagenómica de próxima generación detecta patógenos infecciosos
- Herramienta de diagnóstico identifica rápidamente variantes emergentes del SARS-CoV-2
- Sistema de diagnóstico de hemograma completo y sepsis busca resultados más rápidos, tempranos y fáciles
- Nuevo grupo sanguíneo descubierto ayudará a identificar y tratar a pacientes
- Puntuación de plaquetas sanguíneas detecta el riesgo de ataque cardíaco y accidente cerebrovascular
- Sistema automatizado de sobremesa lleva pruebas de sangre a cualquier persona, en cualquier lugar
- Nuevos analizadores de hematología ofrecen resultados combinados de VSG y CBC/DIFF en 60 segundos
- Método de imágenes mapea conexiones entre células inmunes para predecir supervivencia de pacientes con cáncer
- Herramienta computacional predice resultados de inmunoterapia en cáncer de mama metastásico
- Biomarcador podría predecir respuesta a inmunoterapia en cáncer de hígado
- Prueba epigenética podría determinar eficacia de nuevos tratamientos de inmunoterapia contra mieloma múltiple
- Análisis de sangre predice la supervivencia en pacientes con cáncer de hígado
- Prueba de cabecera de alta precisión diagnostica infección articular periprotésica en cinco minutos
- Enfoque innovador para diagnóstico de infecciones bacterianas permitirá un tratamiento más rápido y eficaz
- Análisis de heces diagnostica endometriosis y ayuda a reducir progresión de la enfermedad
- Plataforma de preparación de muestras de hemocultivos positivos diseñada para combatir sepsis y resistencia a antimicrobianos
- Tecnología revolucionaria de detección molecular podría transformar el diagnóstico de enfermedades infecciosas
- Tecnología de diagnóstico basada en nanomateriales controla farmacoterapia en pacientes epilépticos
- Métodos no invasivos detectan exposición al plomo de forma más rápida, sencilla y precisa en POC
- Prueba no invasiva detecta malaria sin muestra sanguínea
- Dispositivo portátil detecta cáncer colorrectal y de próstata en una hora
- Tecnología Light-AI para diagnóstico del cáncer eliminaría necesidad de extracciones de sangre y biopsias tradicionales
- Microbiologics adquiere fabricante de controles de calidad de diagnóstico SensID
- Beckman Coulter se asocia con BioPorto para distribución global de pruebas NGAL para lesiones renales agudas
- Se anuncia nueva fecha y sede del CACLP 2025
- Roche desarrollará nuevas tecnologías de diagnóstico para lesiones cerebrales traumáticas
- LGC Clinical Diagnostics y AccuGenomics colaboran para mejorar precisión de pruebas de cáncer
- Mapeo de células de placa aterosclerótica predice riesgo de accidente cerebrovascular o ataque cardíaco
- Análisis de células inmunes mediante IA predice pronóstico del cáncer de mama
- Técnica de imagenología reduce sesgo del tono de piel en detección del cáncer mamario
- Herramienta de IA "ve" firmas genéticas del cáncer en imágenes de biopsias
- Herramienta de IA identifica nuevas firmas genéticas para personalizar terapias contra cáncer

Expo
 ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunologíaMicrobiología
TecnologíaIndustria
Eventos
Publique su anuncio con nosotros
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunologíaMicrobiología
TecnologíaIndustria
Eventos
Publique su anuncio con nosotros


- Herramienta de diagnóstico identifica múltiples condiciones de salud a partir de una sola gota de sangre
- Un analizador integrado de química e inmunoensayo con extenso menú de ensayos ofrece flexibilidad, escalabilidad y conmutabilidad de datos
- Prueba rápida de fármacos podría mejorar el tratamiento de pacientes que se presentan en el hospital
- Modelo de IA detecta el cáncer a una velocidad relámpago mediante análisis de azúcar
- El primer chip alimentado por sangre ofrece monitoreo de salud en tiempo real
- Panel de biopsia líquida para tratamiento de cánceres pediátricos
- Prueba por punción digital detecta Alzheimer de forma temprana
- Análisis de sangre más inteligentes permiten diagnósticos más rápidos y mejores resultados
- Una única prueba de secuenciación metagenómica de próxima generación detecta patógenos infecciosos
- Herramienta de diagnóstico identifica rápidamente variantes emergentes del SARS-CoV-2
- Sistema de diagnóstico de hemograma completo y sepsis busca resultados más rápidos, tempranos y fáciles
- Nuevo grupo sanguíneo descubierto ayudará a identificar y tratar a pacientes
- Puntuación de plaquetas sanguíneas detecta el riesgo de ataque cardíaco y accidente cerebrovascular
- Sistema automatizado de sobremesa lleva pruebas de sangre a cualquier persona, en cualquier lugar
- Nuevos analizadores de hematología ofrecen resultados combinados de VSG y CBC/DIFF en 60 segundos
- Método de imágenes mapea conexiones entre células inmunes para predecir supervivencia de pacientes con cáncer
- Herramienta computacional predice resultados de inmunoterapia en cáncer de mama metastásico
- Biomarcador podría predecir respuesta a inmunoterapia en cáncer de hígado
- Prueba epigenética podría determinar eficacia de nuevos tratamientos de inmunoterapia contra mieloma múltiple
- Análisis de sangre predice la supervivencia en pacientes con cáncer de hígado
- Prueba de cabecera de alta precisión diagnostica infección articular periprotésica en cinco minutos
- Enfoque innovador para diagnóstico de infecciones bacterianas permitirá un tratamiento más rápido y eficaz
- Análisis de heces diagnostica endometriosis y ayuda a reducir progresión de la enfermedad
- Plataforma de preparación de muestras de hemocultivos positivos diseñada para combatir sepsis y resistencia a antimicrobianos
- Tecnología revolucionaria de detección molecular podría transformar el diagnóstico de enfermedades infecciosas
- Tecnología de diagnóstico basada en nanomateriales controla farmacoterapia en pacientes epilépticos
- Métodos no invasivos detectan exposición al plomo de forma más rápida, sencilla y precisa en POC
- Prueba no invasiva detecta malaria sin muestra sanguínea
- Dispositivo portátil detecta cáncer colorrectal y de próstata en una hora
- Tecnología Light-AI para diagnóstico del cáncer eliminaría necesidad de extracciones de sangre y biopsias tradicionales
- Microbiologics adquiere fabricante de controles de calidad de diagnóstico SensID
- Beckman Coulter se asocia con BioPorto para distribución global de pruebas NGAL para lesiones renales agudas
- Se anuncia nueva fecha y sede del CACLP 2025
- Roche desarrollará nuevas tecnologías de diagnóstico para lesiones cerebrales traumáticas
- LGC Clinical Diagnostics y AccuGenomics colaboran para mejorar precisión de pruebas de cáncer
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Mapeo de células de placa aterosclerótica predice riesgo de accidente cerebrovascular o ataque cardíaco
- Análisis de células inmunes mediante IA predice pronóstico del cáncer de mama
- Técnica de imagenología reduce sesgo del tono de piel en detección del cáncer mamario
- Herramienta de IA "ve" firmas genéticas del cáncer en imágenes de biopsias
- Herramienta de IA identifica nuevas firmas genéticas para personalizar terapias contra cáncer




















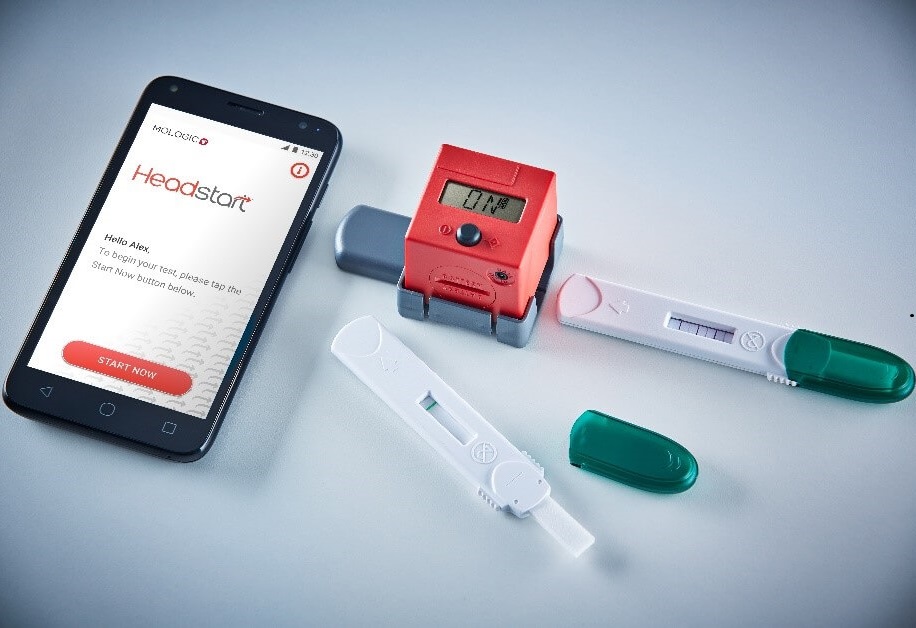

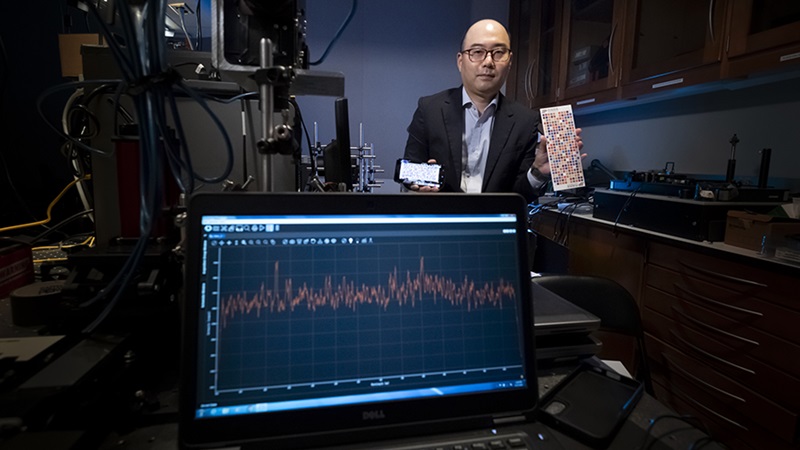
.jpg)
.jpg)
 (1).jpg)
_1_1.jpg)
.jpg)




_1.jpg)




