Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Diagnóstico MolecularHematologíaInmunologíaMicrobiologíaPatologíaTecnologíaIndustria
Eventos
Webinars

- Prueba en el punto de atención basada en IA cuantifica múltiples biomarcadores cardíacos
- Prueba de metabolitos en sangre detecta deterioro cognitivo temprano
- Analizadores automatizados de nueva generación aumentan el rendimiento en química clínica y pruebas de electrolitos
- Análisis de sangre basado en IA detecta múltiples trastornos cerebrales a partir de una sola muestra
- Un ensayo automatizado de NfL respalda el seguimiento de trastornos neurológicos
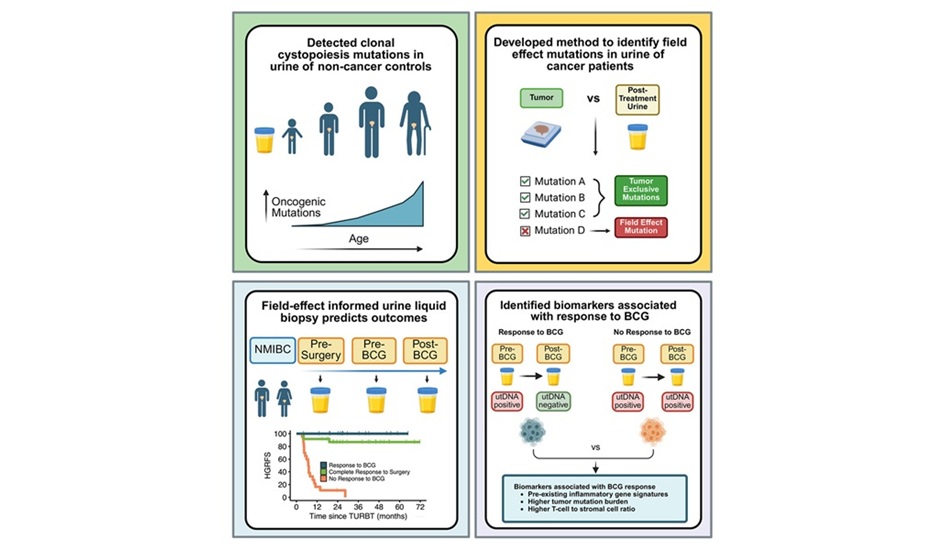
- Prueba de orina no invasiva predice recurrencia tras tratamiento con BCG en cáncer de vejiga
- Mesotelioma en adultos jóvenes vinculado a factores de riesgo genéticos
- Marcador genético predice insuficiencia cardíaca temprana en hipertensión arterial pulmonar
- Firmas inmunológicas en sangre ayudan a estimar el riesgo de cáncer en el síndrome de Lynch
- Análisis de sangre sencillo permite detectar múltiples enfermedades a partir de una sola muestra
- Nuevo ensayo de función plaquetaria permite monitorizar la terapia antiplaquetaria
- Herramienta pronóstica guía el tratamiento personalizado en cáncer hematológico raro
- Plataforma abierta de multiómica identifica subtipos pronósticos en cánceres hematológicos
- Prueba rápida en cartuchos busca ampliar acceso al diagnóstico de trastornos de hemoglobina
- Nuevas directrices buscan mejorar diagnóstico de amiloidosis AL
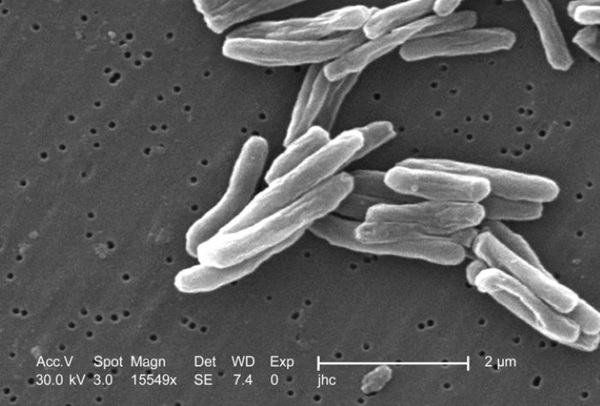
- Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
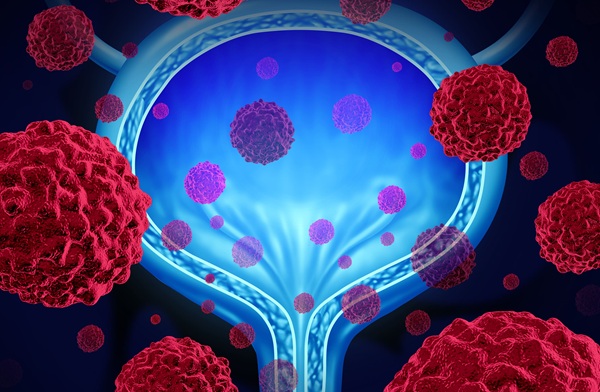
- Identifican una vía inflamatoria que impulsa la resistencia a la inmunoterapia en el cáncer de vejiga
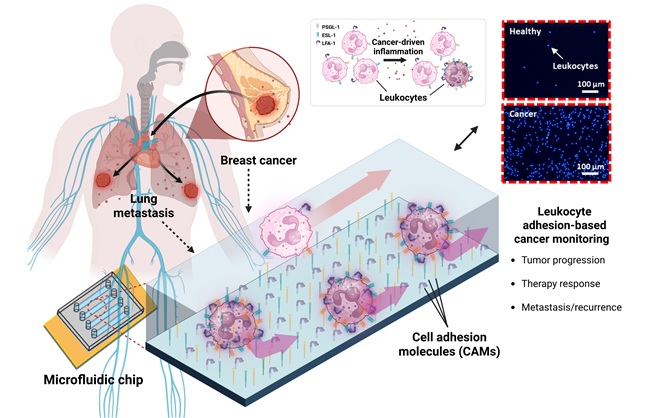
- Chip microfluídico detecta la recurrencia del cáncer a partir de señales de respuesta inmunitaria
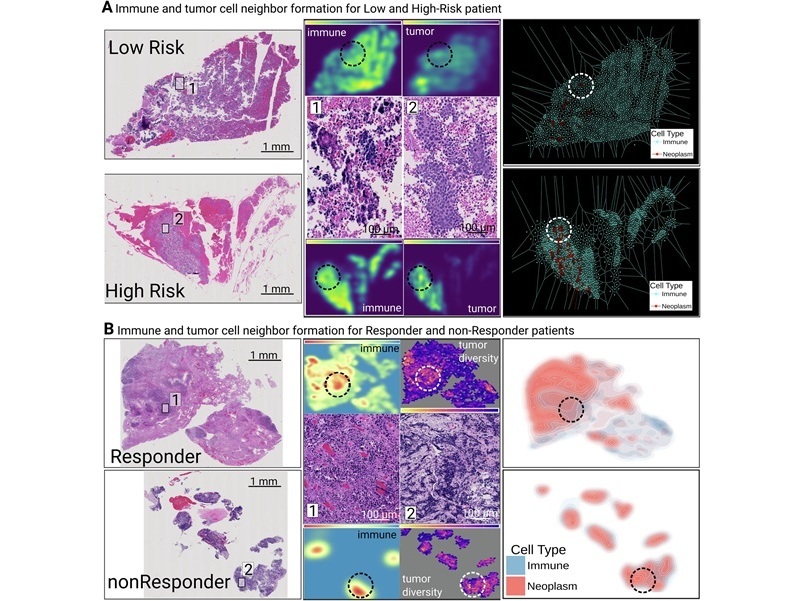
- Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
- Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
- Prueba rápida de orina acelera la selección de antibióticos para infecciones del tracto urinario
- El análisis genómico vincula cepas estreptocócicas emergentes con infecciones específicas
- La OMS respalda las pruebas rápidas en el punto de atención para mejorar la detección de tuberculosis
- Método basado en el aliento distingue infecciones bacterianas de forma rápida
- OMS recomienda pruebas POC, hisopos de lengua y agrupamiento de esputo para diagnóstico de TB
- Nueva herramienta de IA permite seleccionar rápidamente el tratamiento en leucemia pediátrica
- Diseño innovador de espectrometría de masas podría permitir la detección de abundancias ultrabajas
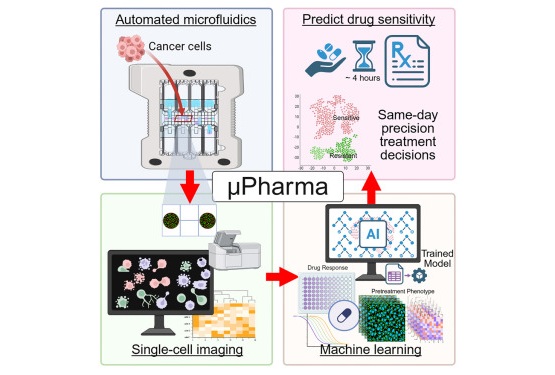
- Biosensor rápido detecta la sensibilidad a fármacos en tumores de mama
- Herramienta en línea apoya el cribado familiar del riesgo de cáncer hereditario
- Sensor de aliento portátil detecta biomarcadores de neumonía en minutos
- Integrated DNA Technologies se expande al ámbito del diagnóstico clínico
- Agilent Technologies adquiere la empresa de diagnóstico patológico Biocare Medical
- Cepheid se une a iniciativa del CDC para fortalecer pruebas detección de pandemias
- QuidelOrtho colabora con Lifotronic para ampliar cartera global de inmunoensayos
- WHX Labs en Dubái resalta habilidades de liderazgo que forman laboratorios de próxima generación
- Herramienta de IA predice respuesta a la quimioterapia en cáncer de pulmón de células pequeñas
- Biomarcador tumoral específico predice respuesta a inmunoterapia neoadyuvante en cáncer gástrico
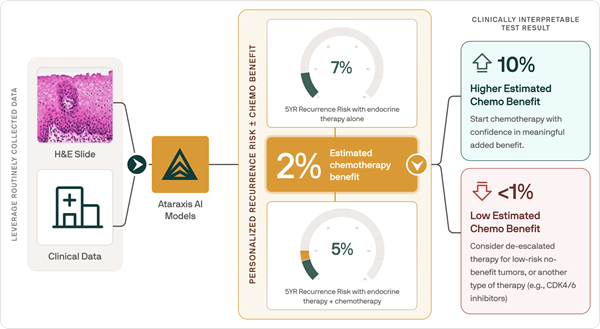
- Nueva prueba de IA predice resultados de quimioterapia específicos para cada paciente con cáncer de mama
- Modelo patológico basado en IA guía las decisiones de quimioterapia en cáncer de mama.
- Prueba genética basada en biopsia predice el riesgo de recurrencia en el adenocarcinoma de pulmón

 Expo
Expo
- Prueba en el punto de atención basada en IA cuantifica múltiples biomarcadores cardíacos
- Prueba de metabolitos en sangre detecta deterioro cognitivo temprano
- Analizadores automatizados de nueva generación aumentan el rendimiento en química clínica y pruebas de electrolitos
- Análisis de sangre basado en IA detecta múltiples trastornos cerebrales a partir de una sola muestra
- Un ensayo automatizado de NfL respalda el seguimiento de trastornos neurológicos
- Prueba de orina no invasiva predice recurrencia tras tratamiento con BCG en cáncer de vejiga
- Mesotelioma en adultos jóvenes vinculado a factores de riesgo genéticos
- Marcador genético predice insuficiencia cardíaca temprana en hipertensión arterial pulmonar
- Firmas inmunológicas en sangre ayudan a estimar el riesgo de cáncer en el síndrome de Lynch
- Análisis de sangre sencillo permite detectar múltiples enfermedades a partir de una sola muestra
- Nuevo ensayo de función plaquetaria permite monitorizar la terapia antiplaquetaria
- Herramienta pronóstica guía el tratamiento personalizado en cáncer hematológico raro
- Plataforma abierta de multiómica identifica subtipos pronósticos en cánceres hematológicos
- Prueba rápida en cartuchos busca ampliar acceso al diagnóstico de trastornos de hemoglobina
- Nuevas directrices buscan mejorar diagnóstico de amiloidosis AL
- Prueba de anticuerpos en sangre identifica tuberculosis activa y distingue la infección latente
- Identifican una vía inflamatoria que impulsa la resistencia a la inmunoterapia en el cáncer de vejiga
- Chip microfluídico detecta la recurrencia del cáncer a partir de señales de respuesta inmunitaria
- Firmas de mutación del cáncer mejoran la predicción de la respuesta a inmunoterapia
- Firma inmunitaria identificada en miastenia gravis resistente al tratamiento
- Prueba rápida de orina acelera la selección de antibióticos para infecciones del tracto urinario
- El análisis genómico vincula cepas estreptocócicas emergentes con infecciones específicas
- La OMS respalda las pruebas rápidas en el punto de atención para mejorar la detección de tuberculosis
- Método basado en el aliento distingue infecciones bacterianas de forma rápida
- OMS recomienda pruebas POC, hisopos de lengua y agrupamiento de esputo para diagnóstico de TB
- Nueva herramienta de IA permite seleccionar rápidamente el tratamiento en leucemia pediátrica
- Diseño innovador de espectrometría de masas podría permitir la detección de abundancias ultrabajas
- Biosensor rápido detecta la sensibilidad a fármacos en tumores de mama
- Herramienta en línea apoya el cribado familiar del riesgo de cáncer hereditario
- Sensor de aliento portátil detecta biomarcadores de neumonía en minutos
- Integrated DNA Technologies se expande al ámbito del diagnóstico clínico
- Agilent Technologies adquiere la empresa de diagnóstico patológico Biocare Medical
- Cepheid se une a iniciativa del CDC para fortalecer pruebas detección de pandemias
- QuidelOrtho colabora con Lifotronic para ampliar cartera global de inmunoensayos
- WHX Labs en Dubái resalta habilidades de liderazgo que forman laboratorios de próxima generación
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Herramienta de IA predice respuesta a la quimioterapia en cáncer de pulmón de células pequeñas
- Biomarcador tumoral específico predice respuesta a inmunoterapia neoadyuvante en cáncer gástrico
- Nueva prueba de IA predice resultados de quimioterapia específicos para cada paciente con cáncer de mama
- Modelo patológico basado en IA guía las decisiones de quimioterapia en cáncer de mama.
- Prueba genética basada en biopsia predice el riesgo de recurrencia en el adenocarcinoma de pulmón








.jpg)









_image.png)