Expo
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunología
PatologíaTecnologíaIndustria
Eventos

- Avance en biodetección abre camino a nuevos métodos de detección temprana de enfermedades
- Nueva prueba de saliva identifica sobredosis de paracetamol
- Dispositivo de pruebas de saliva predice la insuficiencia cardíaca en 15 minutos
- Herramienta de diagnóstico identifica múltiples condiciones de salud a partir de una sola gota de sangre
- Un analizador integrado de química e inmunoensayo con extenso menú de ensayos ofrece flexibilidad, escalabilidad y conmutabilidad de datos
- Análisis podría detectar tipo de ictus antes de llegar al hospital
- Análisis de sangre identifica pacientes con patología amiloide asociada al Alzheimer
- Herramienta detecta variantes de rápida propagación del SARS-COV-2
- Nueva prueba de biopsia evalúa riesgo de cáncer de próstata agresivo en etapa temprana
- Prueba de orina detecta cáncer de próstata agresivo
- Tecnología de recuento de plaquetas ayudará a prevenir errores de diagnóstico
- Sistema de hemostasia POC podría prevenir muertes maternas
- Nueva prueba evalúa capacidad de los glóbulos rojos para transportar oxígeno midiendo su forma
- Pruebas de hemograma completo personalizadas ayudarían a diagnosticar enfermedades en etapa temprana
- Prueba no invasiva determina estado RhD fetal a partir del plasma materno
- Nuevo descubrimiento en células inmunes de la sangre abre camino a prueba diagnóstica para Parkinson
- Herramienta de IA utiliza análisis de sangre rutinario para predecir respuesta a inmunoterapia en cáncer
- Análisis de sangre puede predecir tiempo de inmunidad a la vacuna
- Dispositivo basado en chip microfluídico mide inmunidad viral
- Simple análisis sanguíneo podría detectar resistencia a fármacos en cáncer de ovario
- Ensayo de liberación de interferón-γ es eficaz en pacientes con EPOC y tuberculosis pulmonar
- Nuevas pruebas en punto de atención ayudan a reducir uso excesivo de antibióticos
- Prueba de sepsis rápida permite diferenciar infecciones bacterianas, virales y enfermedades no infecciosas
- Prueba CRISPR-TB permite diagnóstico temprano de enfermedad y cribado de la población
- Panel sindrómico ofrece respuestas rápidas para diagnóstico ambulatorio de enfermedades gastrointestinales
- Plataforma de laboratorio en chip agilizar diagnóstico del cáncer
- Plataforma de biosensores detecta simultáneamente vitamina C y SARS-CoV-2
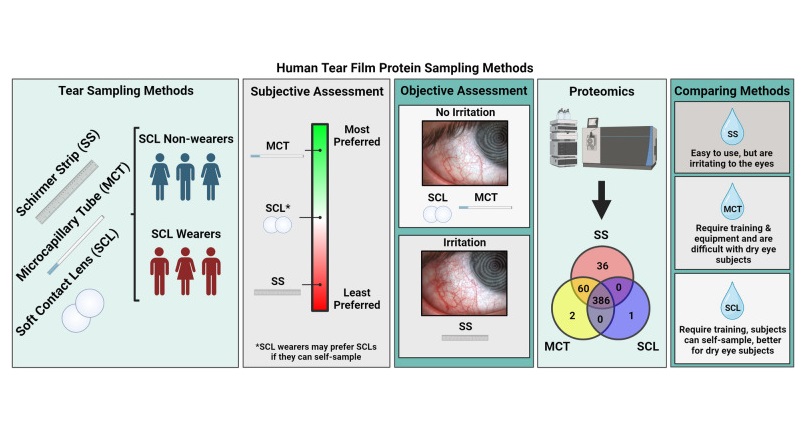
- Nuevo método analiza lágrimas para detectar enfermedades de forma temprana
- Sensores basados en FET abren camino a dispositivos de diagnóstico portátiles para detectar múltiples enfermedades
- Biosensor basado en papel para detectar glucosa mediante sudor revoluciona tratamiento de diabetes
- Medlab Middle East mira hacia el futuro de los laboratorios
- Medix Biochemica adquiere Candor Bioscience, desarrollador de soluciones de inmunoensayo
- bioMérieux adquiere SpinChip Diagnostics empresa noruega especializada en inmunoensayos
- Danaher se asocia con Innovaccer para ofrecer novedosas soluciones digitales y de diagnóstico
- OraSure Technologies adquiere Sherlock Biosciences
- Análisis de sangre mide lipoproteína (a) en unidades molares para mejor evaluación del riesgo cardiovascular
- Secuenciación de lectura larga mejora tasa de diagnóstico de enfermedades raras
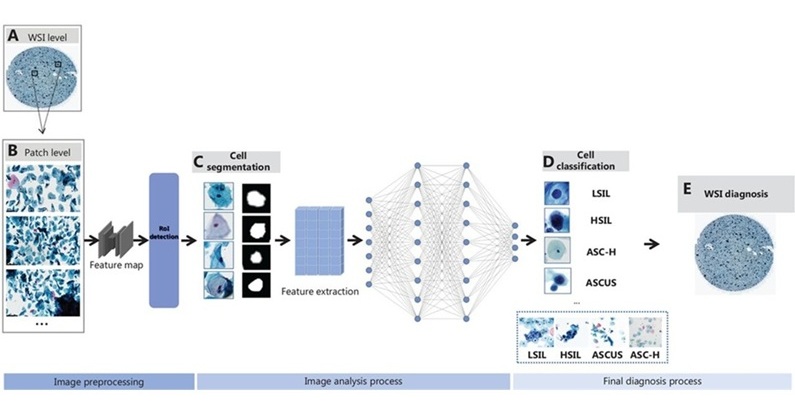
- IA mejora detección del cáncer de cuello uterino
- Algoritmo permite detección no invasiva del esófago de Barrett y cáncer de esófago
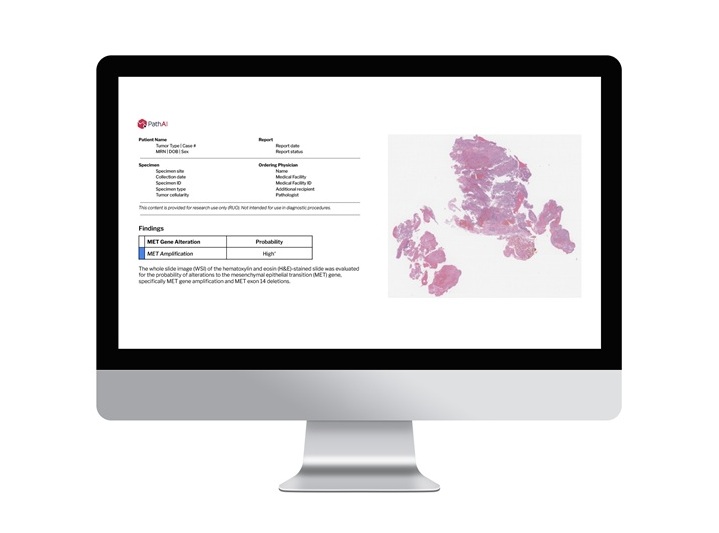
- Herramienta de IA analiza 30.000 puntos de datos por píxel de imágenes médicas en búsqueda de cáncer

Expo
 ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunología
PatologíaTecnologíaIndustria
Eventos
Publique su anuncio con nosotros
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
ver canal
Química ClínicaDiagnóstico MolecularHematologíaInmunología
PatologíaTecnologíaIndustria
Eventos
Publique su anuncio con nosotros


- Avance en biodetección abre camino a nuevos métodos de detección temprana de enfermedades
- Nueva prueba de saliva identifica sobredosis de paracetamol
- Dispositivo de pruebas de saliva predice la insuficiencia cardíaca en 15 minutos
- Herramienta de diagnóstico identifica múltiples condiciones de salud a partir de una sola gota de sangre
- Un analizador integrado de química e inmunoensayo con extenso menú de ensayos ofrece flexibilidad, escalabilidad y conmutabilidad de datos
- Análisis podría detectar tipo de ictus antes de llegar al hospital
- Análisis de sangre identifica pacientes con patología amiloide asociada al Alzheimer
- Herramienta detecta variantes de rápida propagación del SARS-COV-2
- Nueva prueba de biopsia evalúa riesgo de cáncer de próstata agresivo en etapa temprana
- Prueba de orina detecta cáncer de próstata agresivo
- Tecnología de recuento de plaquetas ayudará a prevenir errores de diagnóstico
- Sistema de hemostasia POC podría prevenir muertes maternas
- Nueva prueba evalúa capacidad de los glóbulos rojos para transportar oxígeno midiendo su forma
- Pruebas de hemograma completo personalizadas ayudarían a diagnosticar enfermedades en etapa temprana
- Prueba no invasiva determina estado RhD fetal a partir del plasma materno
- Nuevo descubrimiento en células inmunes de la sangre abre camino a prueba diagnóstica para Parkinson
- Herramienta de IA utiliza análisis de sangre rutinario para predecir respuesta a inmunoterapia en cáncer
- Análisis de sangre puede predecir tiempo de inmunidad a la vacuna
- Dispositivo basado en chip microfluídico mide inmunidad viral
- Simple análisis sanguíneo podría detectar resistencia a fármacos en cáncer de ovario
- Ensayo de liberación de interferón-γ es eficaz en pacientes con EPOC y tuberculosis pulmonar
- Nuevas pruebas en punto de atención ayudan a reducir uso excesivo de antibióticos
- Prueba de sepsis rápida permite diferenciar infecciones bacterianas, virales y enfermedades no infecciosas
- Prueba CRISPR-TB permite diagnóstico temprano de enfermedad y cribado de la población
- Panel sindrómico ofrece respuestas rápidas para diagnóstico ambulatorio de enfermedades gastrointestinales
- Plataforma de laboratorio en chip agilizar diagnóstico del cáncer
- Plataforma de biosensores detecta simultáneamente vitamina C y SARS-CoV-2
- Nuevo método analiza lágrimas para detectar enfermedades de forma temprana
- Sensores basados en FET abren camino a dispositivos de diagnóstico portátiles para detectar múltiples enfermedades
- Biosensor basado en papel para detectar glucosa mediante sudor revoluciona tratamiento de diabetes
- Medlab Middle East mira hacia el futuro de los laboratorios
- Medix Biochemica adquiere Candor Bioscience, desarrollador de soluciones de inmunoensayo
- bioMérieux adquiere SpinChip Diagnostics empresa noruega especializada en inmunoensayos
- Danaher se asocia con Innovaccer para ofrecer novedosas soluciones digitales y de diagnóstico
- OraSure Technologies adquiere Sherlock Biosciences
- Encuentran etiologías de COVID prolongada en muestras de sangre con infección aguda
- Dispositivo novedoso detecta anticuerpos contra la COVID-19 en cinco minutos
- Prueba para COVID-19 mediante CRISPR detecta SARS-CoV-2 en 30 minutos usando tijeras genéticas
- Asocian disbiosis del microbioma intestinal con la COVID-19
- Validan prueba rápida novedosa de antígeno para el SARS-CoV-2 con respecto a su exactitud diagnóstica
- Análisis de sangre mide lipoproteína (a) en unidades molares para mejor evaluación del riesgo cardiovascular
- Secuenciación de lectura larga mejora tasa de diagnóstico de enfermedades raras
- IA mejora detección del cáncer de cuello uterino
- Algoritmo permite detección no invasiva del esófago de Barrett y cáncer de esófago
- Herramienta de IA analiza 30.000 puntos de datos por píxel de imágenes médicas en búsqueda de cáncer













 ELISA.jpg)